Antigènes
Antigènes
Le système ABO fut le premier système découvert par Landsteiner en 1901. Ce système n'est pas spécifique aux globules rouges car il est également présent au niveau des tissus et joue un rôle dans le rejet des transplantations rénales par exemple. Au niveau érythrocytaire, les antigènes ABO sont essentiellement exprimés sur la bande 3, la bande 4.5 et la glycoprotéine RhAG. Il est constitué de 4 antigènes : A / B / A,B / A1. Le groupe O est défini par l'absence de ces 4 antigènes.
Génétique
Les gènes ABO se situent sur le chromosome 9. Chaque locus du chromosome 9 est occupé par un gène A, B ou O. Le gène O est considéré comme un gène amorphe car il ne conduit à aucun antigène détectable sur les globules rouges.
Biosynthèse
Les antigènes A et B sont construits à partir d'enzymes spécifiques : les glycosyltransférases A et B. Ces glycotransférases sont le produit des gènes A et B. Ce ne sont donc pas les gènes qui produisent directement l'antigène. Le gène A code pour une α-N-acétylgalactosaminyltransférase alors que le gène B code pour une α-D-galactosyltransférase.
La biosynthèse des antigènes du système ABO s'effectue dans l'appareil de Golgi et le réticulum endoplasmique. L'initialisation s'effectue à partir d'une protéine ou d'un lipide, où une unité saccharidique va s'ancrer afin de débuter l'élongation. Lors de l'élongation, un enchainement de disaccharides de bases linéaires ou branchées va se fixer sur l'unité saccharidique (antigène I). On obtient ainsi un disaccharide terminal de type 2 (Galβ1-4 GlcNAc-R). Ensuite, l'enzyme fabriquée par le gène H va fixer un Fucose sur le carbone 2 du galactose terminal du disaccharide de type 2 afin de former un trisaccharide formant l'antigène H. Enfin, les glycosyltransférases A et/ou B vont fixer sur le carbone 3 du galactose terminal du disaccharide de type 2 un N-acétyl-D-galactosamine et/ou un D-galactose correspondant, formant l'antigène A ou B. Ce tetrasaccharide va migrer dans une des vésicules golgiennes vers la membrane cellulaire puis s'ancrer dans la membrane grâce à la protéine ou au lipide de départ.
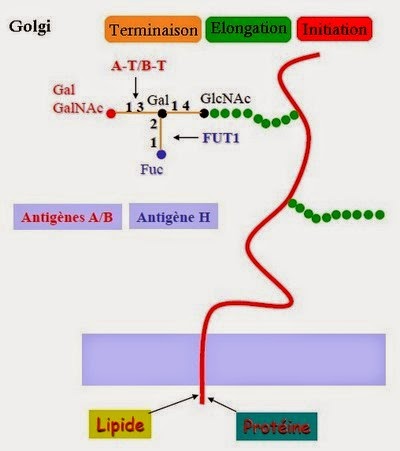
Biochimie
Les antigènes ABO sont localisés sur la partie terminale des chaînes saccharidiques, plus ou moins longues et plus ou moins branchées, reliées à des protéines ou à des lipides membranaires (glycoprotéines ou glycolipides).
L'antigène A est une N-acetylgalactosamine alors que l'antigène B est une D-galactose.
Phénotypes
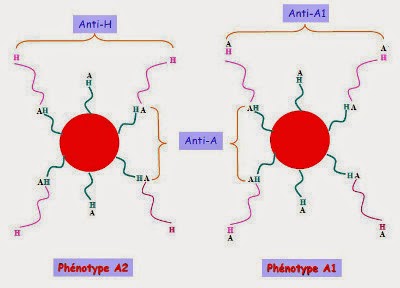
Phénotype A1 et A2 :
Une hématie de groupe A exprime deux types de substrats H (type 2 et type 3). Si les enzymes A1 et A2 ont la capacité de fixer l'antigène A sur le H de type 2, seule l'enzyme A1 a la capacité de fixer l'antigène A sur l'antigène H de type 3; le gène A2 ayant 21 acides aminés supplémentaires conduisant à cette perte de capacité.
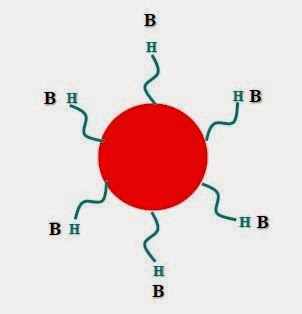
Phénotype B:
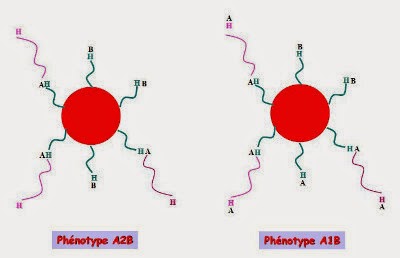
Phénotype AB :
Phénotype O :
Phénotype A faible et B faible :
Les hématies A faibles ont une réactivité inférieure à celle des hématies A2. Ces phénotypes faibles sont dus soit à une baisse d'activité enzyme de la glycosyltransférase, soit à une diminution de la production d'enzyme. En dehors du phénotype A3, les hématies A faibles ne sont pas agglutinées par de nombreux anti-A et/ou anti-A,B et leur détection est le plus souvent le fait d'une discordance de groupage ABO; il en est de même pour les B faibles. L'identification d'un phénotype A faible et B faible est relativement simple si l'on utilise l'agglutination, la fixation-élution, l'étude des anticorps irréguliers et l'étude de la salive. La biologie moleculaire peut être également utilisée.
| Beth-Vincent | Simonin | ||||||
| Groupe | anti-A | anti-B | anti-AB | A1 | A2 | B | O |
| A3 | ++/- | - | ++/- | + ou - | - | +++ | - |
| Ax | (+) | - | + | + | - | +++ | - |
| Aend | (+)/- | - | (+)/- | + ou - | (+) ou - | +++ | - |
| Am | - | - | - | - | - | +++ | - |
| Ael | - | - | - | +++ | ++ ou + | +++ | - |
| Ay | - | - | - | - | - | +++ | - |
| Abantu | + | - | + | + | - | +++ | - |
| Alae | - | - | - | - | - | +++ | - |
| Afinn | (+) | - | (+) | + | - | +++ | - |
| B3 | - | ++/- | ++/- | +++ | ++ | - | - |
| Bx | (+) ou - | - | (+) | +++ | ++ | + | - |
| Bm | - | - | - | +++ | ++ | - | - |
| Bel | - | - | - | +++ | ++ | (+) ou - | - |
D'autres phénotypes A faibles liés à des allèles spécifiques ne correspondent pas à cette classification. Ils sont définis par le terme Aw (Aw-1, Aw-2, Aw-3, Aw-4, Aw-5). L'antigène B possède ces mêmes types de variantes, notées : Bw (Bw-1, Bw-2, Bw-3, Bw-4, Bw-5, Bw-6, Bw-7, Bw-8, Bw-9).
Phénotype Amos et Bmos :
En 1975, Mash décrit les cas de 5 individus dont deux d'une même famille qui présentent dans leur sang des hématies de groupe A et des hématies de groupe B, sans explication de la possibilité d'avoir une double population. Ce phénomène est décrit comme permanent.
Phénotype cis-AB :
Les phénotypes cis-AB sont caractérisés par un groupe AB mais provenant d'un même chromosome en position cis alors que les patients AB ont généralement un chromosome A et un chromosome B en position trans. Ce phénotype cis-AB a été découvert à la suite de la naissance d'un enfant O de parents O et AB. En fait, le gène cis-AB code pour une enzyme hybride qui possède l'activité enzymatique de A et de B conduisant à la fixation de l'antigène A et de l'antigène B sur les globules rouges.
Le phénotype cis-AB est caractérisé par un déséquilibre entre la réactivité des antigènes A (réactivité normale) et des antigènes B (réactivité faible), et un excès de substance H, analogue à celle d'un phénotype A2 voire O. Ainsi, il a été défini 3 phénotypes principaux : cis-A2B, cis-A1B3 et cis-A2B3. le plus fréquemment rencontré est le phénotype cis-A2B3.
B acquis
Lors du cancer du colon infecté avec septicémie, certains malades de groupe A1 voient apparaitre sur leurs globules rouges une réactivité B. On appelle cela un antigène B acquis. Ce phénomène est dû à une déacétylation du tétrasaccharide A conduisant à une galactosamine. Cette galactosamine a une structure proche de la galactose ce qui conduit à des réactions croisées avec l'anti-B. La réglementation a imposé que les antisérums anti-B ne reconnaissent pas les antigène B-acquis. Ce phénomène n'est que transitoire et ne dure que le temps de la vie des hématies ayant subi l'action de cette enzyme bactérienne.
Il existe le même phénomène pour l'antigène A, lorsque des hématies polyagglutinables de type Tn, dont le sucre dominant est une N-acétylgalactosamine (antigène A), réagissent avec les anti-A. On obtient ainsi le phénotype A acquis.
Modification antigénique
Lors de pathologies malignes hématologiques, certains individus perdent leur antigène ABO conduisant à la présence d'une double population de globules rouges dans leur sang. Ce déficit en antigène A ou B est lié au déficit de l'enzyme correspondante.
Répartition dans le monde
| Fréquence | Caucasiens | Africains | Arabes | Indiens | Chinois | Japonais | Brésiliens |
| A | 43% | 27% | 27% | 21% | 28% | 39% | 34% |
| B | 9% | 20% | 16% | 40% | 29% | 22% | 14% |
| AB | 4% | 4% | 4% | 9% | 9% | 10% | 3% |
| O | 44% | 49% | 54% | 29% | 34% | 29% | 49% |
| Dans certains groupes Sud-Amérindiens, 100% sont O | |||||||
 Anticorps
Anticorps
Anti-A et anti-B
Lorsque le système ABO a été découvert, les anticorps anti-A et anti-B étaient considérés comme des molécules d'apparition naturelle, sans stimulation par l'antigène correspondant. Cette idée était un défi aux lois classiques de l'immunologie, d'où le terme d'anticorps naturel. On sait maintenant que les antigènes A et B sont très largement présents dans la nature et notamment au niveau de la membrane des bactéries intestinales et ceci est à l'origine de la formation des anticorps anti-A ou/et anti-B des individus.
Les anti-A et les anti-B sont essentiellement des IgM ou un mélange d'IgM et d'IgG. Ces anticorps sont présents dans le plasma dès lors que l'antigène n'est pas présent sur le globule rouge. Ces anticorps apparaissent généralement dans les 6 premiers mois de la vie. Il arrive parfois qu'on observe la présence de ces anticorps à la naissance.
La concentration de ces anticorps baisse lors du vieillessement et lors de pathologies tel que les myélomes, la maladie de Waldenström, ou la leucémie lymphoïde chronique. Elles peuvent également augmenter lors de maladies auto-immunes ou lors d'hépatite chronique tel que la cirrhose. Une absence totale d'anticorps ABO est également observée dans des situations pathologiques d'immunodépression, en cas de greffe de cellules souches hématopoïétiques ou chez les jumeaux dizygotes.
En dehors des anticorps naturels, il existe également des anticorps de type IgG et IgA qui ont un pouvoir hémolytique puissant. Ce sont des anti-A et des anti-B immuns. Ils sont très actifs à 37°C et sont produits à la suite de vaccinations, sérothérapie, infections ou à la suite d'une grossesse.
Anti-A,B
L'anti-A,B est présent chez les individus de groupe O. Ce sont essentiellement des IgM bien que parfois cela puisse être des IgG ou IgA. Ces anticorps réagissent contre les antigènes A et les antigènes B.
Anti-A1
L'anti-A1 est observé chez les individus A2 et A2B, mais également chez les individus B et O. C'est un anticorps irrégulier car il n'est pas systématiquement présent chez l'individu. Ce sont des IgM qui sont présents chez environ 2% des individus de groupe A2 et 25% des groupes A2B.
Auto-Anticorps
Les auto-anticorps anti-A et anti-B sont rares. Ce sont des IgM actifs à 4°C.
Incidences cliniques
Les anticorps du système ABO sont une barrière essentielle lors de transfusion sanguine. En effet, les anticorps du receveur peuvent, après fixation sur les hématies incompatibles transfusées, aboutir à un choc hémolytique avec Coagulation Intra-Vasculaire Disséminée (CIVD). Les anticorps ABO sont également responsables de Maladie Hémolytique du Nouveau-Né (MHNN). Cette pathologie se voit surtout chez les nouveau-nés de mère O car les sujets O présentent une proportion plus importante d'anticorps de type IgG.
Si les incompatibilités foetomaternelles ABO sont fréquentes, elles ne nécessitent que rarement un traitement. Il semble que cela soit lié à une faible densité antigénique des hématies foetales, ainsi qu'à la présence de substances solubles neutralisantes présentes dans le plasma de l'enfant. De plus, le déficit en complément dans le plasma néonatal pourrait aussi expliquer la rareté de la MHNN par incompatibilité ABO dans la mesure où l'activité hémolytique de ces IgG est complément dépendante.